2019年,71岁的Marylou Barton被诊断为恶性胸膜间皮瘤(一种罕见且侵袭性极强的癌症),并被告知可能只有一年左右的生命时,她和女儿在医生的办公室里相拥而泣。传统的治疗似乎已无路可走。然而,一次勇敢的尝试改变了一切。她参与了一项创新CAR-T细胞疗法临床试验,五年过去了,Marylou依然健在,享受着与女儿、孙辈共度的时光,并四处旅行。
图片来源于MSK
Marylou的故事并非孤例。它象征着CAR-T细胞疗法-这个在白血病、淋巴瘤等血液肿瘤中创造“治愈”奇迹的明星技术,正在向占所有癌症90%以上的实体瘤领域发起总攻。尽管前路充满挑战,但曙光已现,一系列革命性的策略正在将不可能变为可能。
关于CAR-T疗法
CAR-T细胞疗法的核心原理是通过基因工程改造患者自身的T细胞,使其表达能够识别癌细胞表面特定抗原的嵌合抗原受体。虽然CAR-T细胞疗法并非对所有人都有效,但对于一些晚期癌症患者来说,它可以完全根除他们的疾病,且效果往往能持续很长时间。
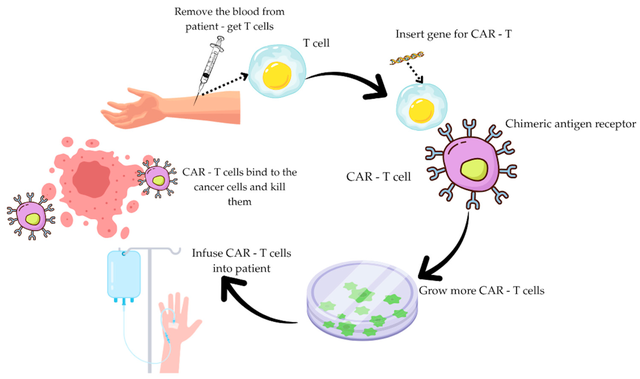
CAR-T疗法与其他癌症治疗方法的不同之处在于,它是由患者自身的T细胞制成的,而T细胞是人体清除受感染细胞及其他病变细胞的重要力量。制备CAR-T疗法的第一步是从患者身上采集血液,并分离出T细胞。然后将这些细胞送往实验室,在那里,通过基因工程改造,使它们表面产生一种称为嵌合抗原受体的特殊蛋白质。
CAR有助于细胞锁定癌细胞(以及一些正常细胞)上存在的特定蛋白质,即抗原。它们还能增强T细胞杀死癌细胞的能力。
接下来,这些经过改造的T细胞被培养或"扩增",直到数量达到数亿。这些扩增后的细胞就是最终的CAR-T细胞疗法产品,它们被送回医院,通过一次输注回输给患者。输注后,T细胞将在患者体内继续扩增,并在其特殊受体的引导下,杀死表面带有目标抗原的任何癌细胞。
破冰实体瘤:创新策略初显成效
与CAR-T细胞疗法在血液癌症方面取得的进展相比,开发用于实体瘤的疗法进展较为缓慢。为了打破实体瘤屏障,全球科学家正在通过多种创新策略寻求突破。
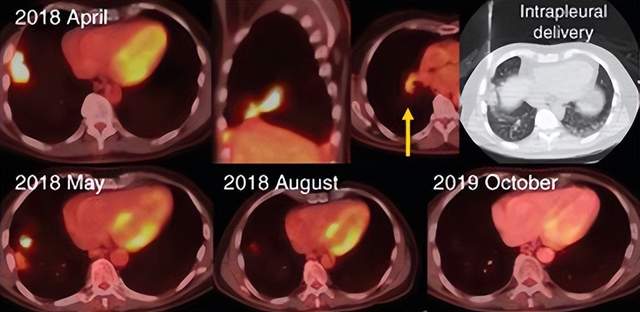
纪念斯隆凯特琳癌症中心研究人员于2021年在《Cancer Discov》发表了CAR-T细胞疗法联合帕博利珠单抗用于恶性胸膜疾病(包括转移性肺癌和乳腺癌以及恶性胸膜间皮瘤)的I期临床试验结果。这项研究创新性地采用了区域性给药联合免疫检查点抑制剂的策略,研究显示:患者的中位总生存期达到23.9个月,1年生存率高达83%。更值得关注的是,一名恶性胸膜间皮瘤(MPM)患者联合治疗后靶病灶减少了78%,并且持续缓解了26个月。另有8名患者疾病稳定(SD)维持了≥6个月,且生活质量良好,长时间无需后续治疗。
中国力量崛起:多项CAR-T成果领跑全球
在全球CAR-T疗法攻克实体瘤的征程中,中国科研力量正发挥着越来越重要的作用。
科济药业CT041
科济药业的CT041是一种靶向Claudin18.2的CAR-T产品,在胰腺导管腺癌(PDAC)中,高达83.3%的患者在术后9个月仍旧无病生存。并且这些产生积极反应的患者关键肿瘤标志物CA19-9水平也得到显著下降,降幅范围为51.3%-96.1%。
浙大一院PC13
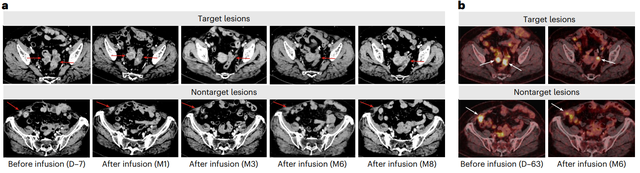
浙江大学医学院附属第一医院方维佳教授团队的研究显示,一种低氧响应型CEA靶向CAR-T细胞药物(PC13)在43例经多线治疗失败的MSS型晚期实体瘤患者中展现出良好治疗潜力,其中一名患者靶病灶最长直径总和减少了75.98%,且在6个月随访时一个靶病灶完全消失。
易慕峰IMC002
易慕峰生物自主研发的靶向Claudin18.2的CAR-T细胞疗法IMC002,在晚期胃癌/胃食管结合部癌患者中展现出了令人鼓舞的疗效:客观缓解率(ORR)达到66.7%,疾病控制率(DCR)高达93.3%。
目前,已有多种CAR-T产品进入临床研发阶段,覆盖了肺癌、肝癌、肾癌、结直肠癌等癌种。这些进展为实体瘤患者提供了更多治疗选择。
值得注意的是,尽管取得了令人鼓舞的进展,但目前CAR-T治疗实体瘤仍处于临床试验阶段,不同靶点、不同癌种的疗效差异较大。且CAR-T疗法费用较高,国内已上市的CAR-T产品定价在100-120万元人民币左右。更加需要了解的是,CAR-T疗法可能引起细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。因此在接受CAR-T治疗之前,患者和家庭需要与医疗团队进行深入、全面的沟通与评估。
结语
随着CAR-T疗法在实体瘤领域的不断突破,更多癌症患者将有机会像Marylou一样,重新拥抱生活的美好。从胸膜间皮瘤到肺癌、肝癌、胰腺癌,CAR-T这一创新疗法正在为曾经被视为“绝症”的疾病带来转机。尽管大部分新型CAR-T疗法仍处于临床试验阶段,但对于实体瘤患者而言,这意味着即使在传统治疗失败后,仍有可能通过CAR-T等新型免疫治疗获得长期控制甚至治愈的机会。