纳米抗体(nanobody,Nb)作为生物制药领域的新型 “精准工具”,其独特功能源于两类核心来源 —— 骆驼科动物重链抗体可变区(VHH)与软骨鱼类新型抗原受体免疫球蛋白可变区(VNAR)。这两类纳米抗体虽同属单域抗体片段,却因进化路径与分子结构差异,呈现出各具特色的理化特性与应用潜力。本文将系统解析二者的结构核心、功能机制与共性优势,揭开纳米抗体高效发挥作用的分子密码。
一、骆驼源纳米抗体(VHH 型):结构简化与功能补偿的典范(一)核心结构特征
骆驼源纳米抗体源自重链抗体(HCAb),其结构革新是功能优势的关键:
结构简化机制:与传统单克隆抗体(含两条重链+两条轻链)不同,HCAb 因恒定区 CH1 结构域(constant heavy 1)及轻链恒定区锚定位点的基因突变缺失,天然缺乏轻链,仅由片段结晶区(Fc)直接连接抗原结合区(Fab)构成,而 Fab 区仅含一个 VHH 结构域。
分子量优势:这种结构精简使其相对分子质量比传统抗体减少约 70,000,其中 VHH 结构域的分子量仅 15,000,约为传统抗体的 1/10,结构紧凑且水溶性极佳,不易聚集。
Fc 区功能:HCAb 的 Fc 区虽结构简化,但仍保留与免疫细胞 Fc 受体结合的潜力,可介导抗体依赖的细胞毒作用(ADCC)等效应功能,同时能结合新生 IgG 转运受体(FcRn),适度延长体内半衰期。
(二)功能补偿策略
由于缺乏轻链可变区(VL),骆驼源 VHH 的互补决定区(CDR)数量仅为传统抗体的一半,可能限制抗原结合范围。为突破这一局限,其第一个互补决定区(CDR1)发生显著延长,通过增加抗原接触位点,实现了与传统抗体相当甚至更广泛的抗原识别能力,完美弥补了轻链缺失带来的功能短板。
(三)典型应用案例
凭借高稳定性与低免疫原性,骆驼源 VHH 已在临床转化中崭露头角:2020 年研究证实,源自大羊驼的 VHH 纳米抗体可通过独特方式结合新冠病毒 S 蛋白,实现高效中和;2022 年临床研究显示,基于羊驼 VHH 的 CAR-T 细胞治疗晚期间皮瘤,患者最长生存时间达 22 个月,完全缓解患者持续无瘤生存超 15 个月。
二、软骨鱼源纳米抗体(VNAR 型):极致紧凑与高适应性的代表(一)独特结构设计
软骨鱼类的 IgNAR 衍生 VNAR 纳米抗体,展现出与骆驼源截然不同的结构特征:
恒定区结构:IgNAR 的 Fc 片段由 C1-C5 五个恒定结构域组成,恒定区中富含半胱氨酸残基,可形成稳定的二硫键,为抗体结构提供极强的理化稳定性,使其能耐受极端温度与 pH 环境。
铰链区特性:与骆驼源 HCAb 不同,IgNAR 在 C1 结构域与 VNAR 之间缺乏规范铰链区,分子灵活性主要依赖 C3 与 C4 结构域之间的铰链区调控;部分亚型通过可变剪接缺失 C2、C3 结构域,使 C1 与 C4 直接连接形成柔性铰链区,进一步提升抗原结合适应性。
最小功能单位:VNAR 由 8 条 β 链组成(传统抗体抗原结合区为 10 条),结构更紧凑,分子量仅 12,000,是目前已知最小的功能性抗原结合片段,组织穿透性优势显著。
(二)结构优化潜力
VNAR 具备独特的分子改造空间:通过疏水性氨基酸向亲水性氨基酸的定点突变,可显著提升其水溶性与体内生物相容性,解决小分子抗体片段易聚集的痛点,为规模化生产与临床应用奠定基础。
三、两类纳米抗体的共性优势与核心差异(一)共性核心优势
抗原结合能力:第三互补决定区(CDR3)虽数量减少但长度更长,且富含亲水性氨基酸,既提升溶解度,又增强抗原结合多样性,亲和力与传统抗体相当;
理化稳定性:在极端 pH、蛋白酶存在或高温条件下仍能保持结构稳定,储存与应用场景更广泛;
组织穿透性:纳米级尺寸使其能穿透血脑屏障、肿瘤微环境等传统抗体难以触及的区域,精准识别隐蔽抗原表位;
表达优势:可在原核或真核系统中高效表达,生产成本低、量产潜力大,适合工业化放大。
(二)核心差异对比
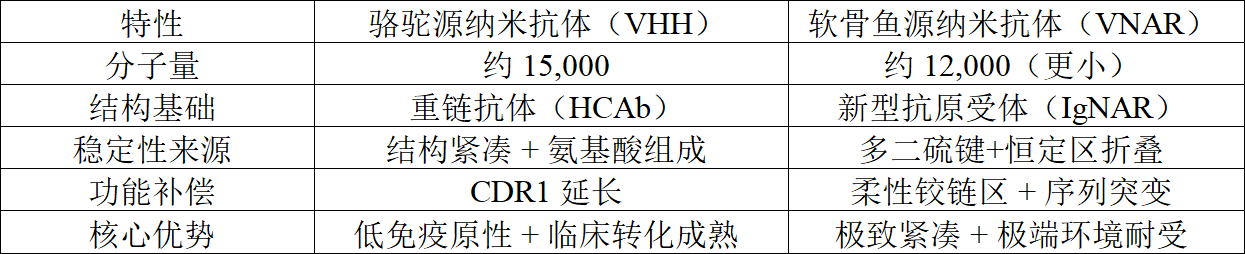
四、总结与应用展望
骆驼源与软骨鱼源纳米抗体,通过不同的进化路径形成了各具特色的结构与功能优势:骆驼源 VHH 凭借低免疫原性与成熟的临床转化经验,成为当前治疗性纳米抗体的主流方向;软骨鱼源 VNAR 则以极致小巧、高稳定性与改造潜力,在特殊环境应用与新型靶点开发中展现出巨大潜力。
随着结构生物学与基因编辑技术的发展,两类纳米抗体的结构将进一步优化,通过人源化改造、多功能融合等策略,有望突破当前免疫原性、半衰期等瓶颈。未来,这些承载着独特结构密码的纳米抗体,将在肿瘤治疗、感染性疾病防控、罕见病诊治等领域发挥更核心作用,推动精准医疗向更高效、更安全的方向迈进。