Rich Gingerelli是一名消防员,他在50岁时第一次被诊断出患有癌症。将近17年后,他开始在一种新武器(CAR-T细胞疗法),利用他自己的T细胞开始了与第二种癌症的斗争。
化疗、复发、移植受挫-濒临崩溃的边缘
那时是1998年,Rich Gingerelli被诊断患有华氏巨球蛋白血症(WM),这是一种罕见的非霍奇金淋巴瘤。幸运的是,这种癌症多年来一直进展缓慢且症状平稳。但在2015年,Rich Gingerelli又被确诊患上弥漫性大B细胞淋巴瘤。
在化疗缓解后,癌症于三年后复发。随后他接受了干细胞移植治疗却再次受挫。Rich Gingerelli回忆表示,那时的他几乎濒临崩溃。
绝境中的新希望:CAR-T疗法带来彻底缓解
但是治疗还要继续进行。幸运的是,当时Rich被介绍给了CAR-T细胞疗法先驱Ran Reshef先生,并在接受治疗后连续两年实现无癌生存。
Rich和妻子特制了以“吃豆人”游戏为主题的蛋糕,象征吞噬癌细胞的寓意。
对于Rich Gingerelli来说,CAR-T疗法带来的不仅是疾病的缓解,更是生活的重启。数年来,随着免疫学和基因工程技术的不断发展,免疫治疗逐渐成为癌症治疗领域的研究热点,其中CAR-T细胞疗法作为免疫治疗的一种形式,引发了极大的关注。尽管CAR-T疗法并非对所有人都有效,但在部分晚期癌症患者身上,它能彻底清除病灶,且疗效往往可持续很长时间。成为了癌症治疗的新希望。
关于CAR-T疗法
嵌合抗原受体(CAR)T细胞疗法是一种“活体药物”,CAR-T细胞源自患者自身的T细胞(一种攻击体内病原体的白细胞)。通过对患者T细胞进行基因改造,使其表达可定向攻击癌细胞的人工受体(CAR)。该受体能引导T细胞精准识别癌细胞(及部分正常细胞)表面的特定抗原蛋白,同时增强T细胞杀伤癌细胞的能力。在通过化疗腾出空间后,这些经过改造的CAR-T细胞会被回输至患者体内,从而精准清除癌细胞。

美国食品和药物管理局(FDA)于2017年批准了第一款CAR-T细胞疗法,此后又有多款CAR-T疗法获批用于治疗成人血液癌症,如非霍奇金淋巴瘤和多发性骨髓瘤。
除已获美国FDA批准上市的CAR-T细胞疗法产品外,其他形式的CAR-T细胞疗法也正在通过临床试验研究其安全性和有效性。
91%肿瘤缓解,12个月生存率达90%!Brexu-cel疗法对套细胞淋巴瘤显示高缓解率
10月29日,美国MD安德森癌症中心研究人员在国际期刊《blood》上分享了他们利用Brexu-cel治疗未接受BTK抑制剂治疗的复发/难治性套细胞淋巴瘤的ZUMA-2研究分析结果。
在所有接受治疗的患者(n=86)中,91%的患者肿瘤缓解,有超过一半的患者(n=63)达到完全缓解(CR),15例部分缓解(PR),3例疾病稳定(SD)。在34例初始缓解为部分缓解/疾病稳定的患者中,16例在中位时间2个月后转为完全缓解。中位无进展生存期(PFS)、缓解持续时间(DOR)、总生存期均未达到,12个月PFS率为75%,12个月DOR率为80%,12个月OS率为90%。
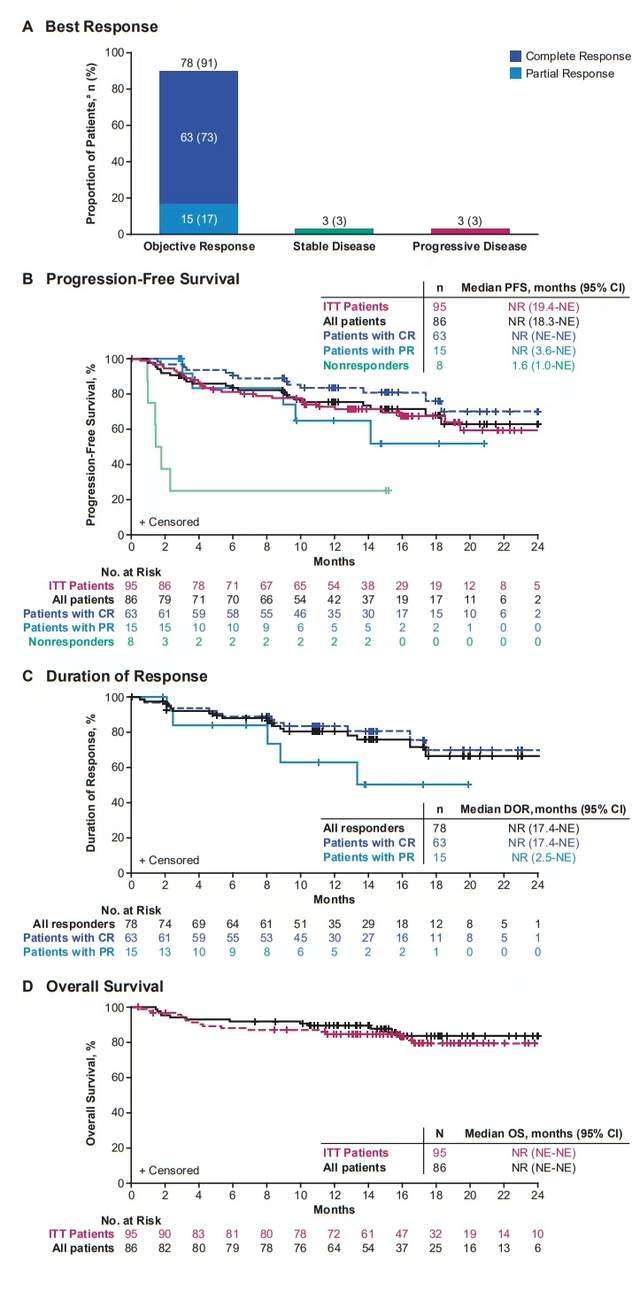
安全性方面,绝大多数患者(88%)出现了与治疗相关的≥3级不良事件,其中包括4例治疗相关的5级事件。与第一队列结果一致,brexu-cel在未接受过BTK抑制剂治疗的患者中展现出高客观缓解率及相似的安全性特征。
这些结果表明brexu-cel在复发/难治性套细胞淋巴瘤中具有有效性。
客观缓解率80%,中位无进展生存期超22个月!国产ssCART-19治疗白血病疗效显著
10月27日,优卡迪生物以及吴德沛教授团队在国际权威血液学期刊《Blood Cancer Journal》分享了ssCART-19在成人难治/复发急性B淋巴细胞白血病(r/r B-ALL)患者中的研究成果。
在17例输注ssCART-19的患者8天疗效评估中,14例患者肿瘤缓解,有8例患者完全缓解(CR)、3例血细胞未完全恢复的完全缓解(CRi)。降低治疗剂量后,临床应答效果得到进一步改善,客观缓解率达到80%。
在中位随访20.1个月的时间里,14例肿瘤缓解患者的中位缓解持续时间(DOR)为25.8个月,且所有患者的中位无进展生存期(PFS)达22.2个月,总生存期(OS)尚未达到。
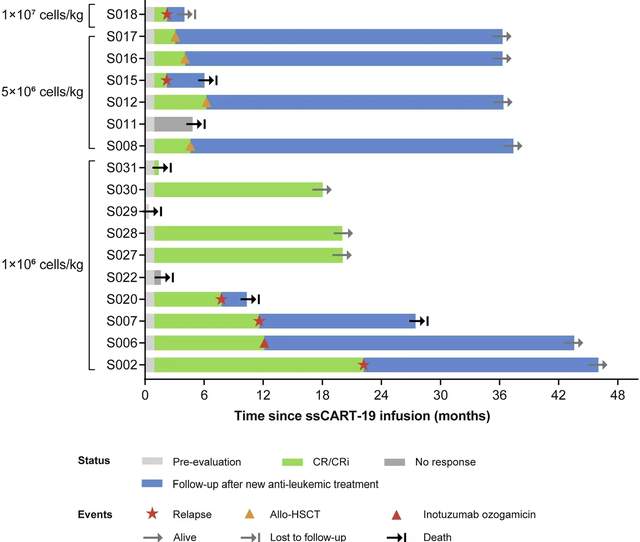
综上可见,CAR-T疗法具有令人鼓舞的临床效果。
患者及家属通常会对CAR-T疗法本身存在一些普遍疑问。为了帮助大家更全面地认识这项疗法,我们接下来对一些常见问题做出解答。
CAR-T疗法适用于哪些患者?
目前,CAR-T细胞疗法可用于患有某些类型的霍奇金淋巴瘤和非霍奇金淋巴瘤、多发性骨髓瘤和白血病的成年患者。同时还在卵巢癌、肾癌、胃癌等实体肿瘤中进行大量临床试验。CAR-T疗法初期仅通过临床试验开展,严苛的入组标准(如年龄限制、无合并症、肝肾功能良好等)将许多患者拒之门外。但Loretta Nastoupil医生的研究证实,不符合试验标准的患者同样能从CAR-T中获益。这一发现极大拓宽了适用人群,尤其为癌症已转移的患者带来生机。
接受CAR-T细胞疗法对患者身体的影响有多大?
CAR-T与我们常规药物不同,因为需要为每位患者个体化定制药物。数据显示,在输注CAR-T细胞前需要进行轻度化疗,以便为细胞腾出生存空间。多数患者接受3-4天化疗后,仅需单次输注细胞即可。输注过程比输血更简便——护士注射微量细胞液即完成治疗。但随后1-2周内,这些"活体药物"会在患者体内扩增,从而实现肿瘤清除,但同时也可能引发细胞因子释放综合征这种类似重度流感的副作用。
CAR-T疗法副作用
与其他癌症治疗一样,CAR-T细胞疗法可能引发副作用。最常见且严重的是细胞因子释放综合征(CRS),即“细胞风暴”。这是由于免疫系统对输注的CAR-T细胞产生过度反应所致。部分患者可能出现类似流感的轻度症状(高热、乏力、全身疼痛),严重者则会出现低血压或组织缺氧,甚至器官衰竭。
早期CRS曾令医学界措手不及,但如今我们发现,原本用于治疗幼年关节炎的托珠单抗能快速逆转多数病例。另一副作用是免疫效应细胞相关神经毒性综合征(ICANS),患者可能出现意识模糊、定向障碍或短暂失语(类似中风症状)。虽然ICANS的成因尚未明确,但临床证实大多数患者数日内可康复,且类固醇治疗对其效果显著。
副作用是否在所有患者中出现?
存在个体差异。约30%-60%患者会出现不同程度的细胞因子释放综合征。轻度症状仅表现为单日发热,重度患者则可能需重症监护。
结语
目前,CAR-T疗法仍有巨大发展空间,尤其在淋巴瘤、多发性骨髓瘤之外的实体瘤治疗方面。但是尽管部分患者经CAR-T治疗后获彻底缓解,但癌症复发仍是挑战。可能原因包括CAR-T细胞耗竭、被普通T细胞排挤,或其他药物干扰。仍旧需要对细胞持久性与效力方面进行持续探索。自首例CAR-T治疗不到十年,该疗法已拯救大量濒临绝境的患者。尽管前路仍长,但众多长期存活案例已证明其非凡价值。随着技术迭代,CAR-T有望为更广泛人群点燃希望之火。