作者:超能文献团队
| 超能文献(https://suppr.wilddata.cn/)
0)引子:一张“变更注册”补正通知,暴露了赛道的真实拥挤度
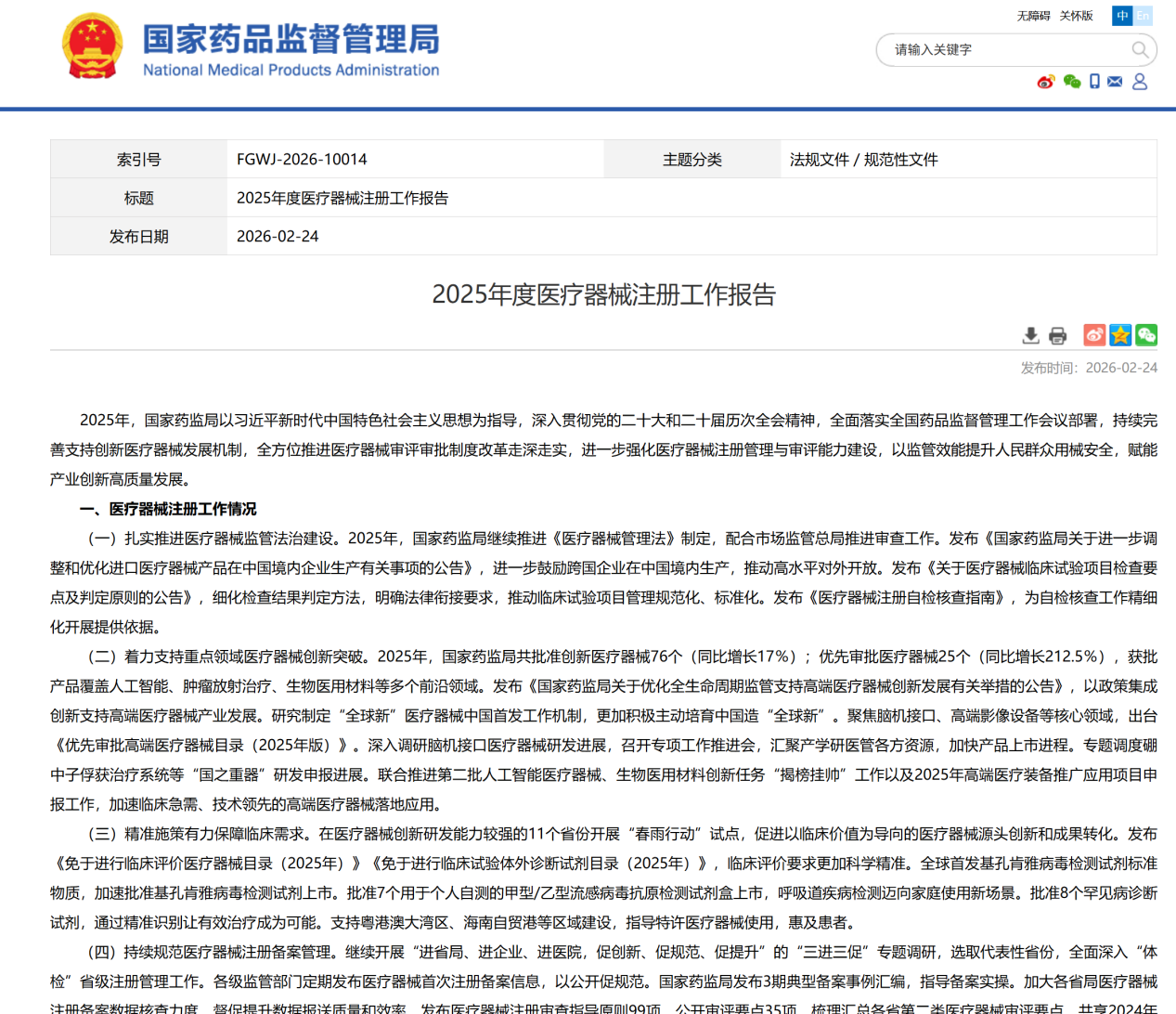
春节后,某三类介入器械企业的注册负责人盯着系统里新弹出的补正通知发愣:产品临床已跑完,上市路径却卡在“变更注册”的一处工艺调整上。她更焦虑的不是补资料本身,而是窗口期——同院科室准备更新器械目录,采购周期一旦错过,后面要等下一轮集采或预算。就在此时,国家药监局于2026年2月24日发布《2025年度医疗器械注册工作报告》,把行业的“拥挤度”量化摊开:全年批准注册14,187项,变更注册5,729项,占比继续抬升。对企业而言,注册不再是终点,而是与临床应用、采购准入并行的耐力赛。1
1)背景:当中国审批“加速”,欧洲却在“排队”
年度注册工作报告的意义,早已不止“汇报成绩”。它更像一张产业运行仪表盘:审批结构是否从“首次注册”转向“延续、变更”,创新通道是否真正提速,监管资源是否跟得上新增需求。
把镜头拉到海外,对比更刺眼。MedTech
Europe的2024年调研显示,在欧盟MDR/IVDR转换中,仍有约11%的医疗器械(MD)企业没有公告机构(Notified
Body)协议;在体外诊断(IVD)领域,中小企业未签约比例仍达37.5%。不少企业的证书被“显著延迟或否决”,与临床/性能评价被挑战直接相关。4这意味着同样面对“临床证据”,欧洲更像是“供给端卡脖子”,而中国则进入“审批与落地同时挤压”的新阶段。
2)核心内容拆解:四年数据里,最该盯住的不是“总量”,而是“结构”
2.1 一张表看清2023—2025:审批在高位,结构在变形
如果只看总量,会得出“稳中有升”的温和结论。真正的信号在结构里:2025年的变更注册达到5,729项,已明显超过首次注册3,402项。企业的主战场正在从“拿证”转向“拿证后怎么持续迭代、怎么不踩雷”。1
2.2 “国产占比抬升”正在发生,但它更像“高风险器械供给扩容”而非简单替代
从受理侧看,境内三类受理量在三年里从7,106项增至8,766项;进口受理量从6,154项降至5,881项,出现此消彼长。1,3这不是一句“国产替代”能概括的变化,更准确的表述是:高风险器械的国产供给,正在更密集地进入审评通道;与此同时,进口端的节奏更敏感,更容易受到全球临床证据、合规成本与本地化策略影响。
2.3 “优先审批”在2025年陡增:监管加速与产业拥挤同步到来
2025年优先审批获批25个,同比增幅达到212.5%,与2024年的8个形成断层。1,2这类跃迁通常意味着两件事同时发生:一端是政策与资源向“临床价值明确”的产品倾斜;另一端是企业集中拥向同一批热点赛道,导致“同质化创新”更快地在临床与采购端短兵相接。
3)多维影响:企业、医院、患者、资本,各自的“压力表”在哪里
对器械企业而言,最直接的影响是研发与注册策略要重排。审批端把“创新”数量推到76个新高后,差异化的关键会更快外溢到注册后环节:临床路径能否嵌入、培训体系是否可复制、耗材与设备的组合是否符合DRG/DIP控费逻辑。审批加速并不会自动换来采购加速,反而可能让“拿证即亏损”的产品更早暴露。1
对医院而言,新增与迭代产品的“评估工作量”被动上升。2024—2025两年,仅变更注册就从5,048增至5,729。1,2这类变更往往涉及工艺、关键性能或适用范围的边界,医院器械管理、临床科室与采购部门需要更快形成“证据审查—试用—培训—质控—复盘”的闭环,否则新器械更容易沦为库房里的“沉默资产”。
对患者而言,潜在收益来自两条路径:一是更多创新器械进入临床选择集;二是国产高风险器械供给增加,长期有望改善可及性与供给稳定性。但现实约束同样明确:支付端控费、院内预算、以及对真实世界效果的持续评估,会决定“能用”与“用得起”之间的距离。1
对投资者而言,2025年优先审批数量的跃迁更像一个分水岭。它提示市场:监管鼓励“临床价值+合规能力”的组合,而不是“讲故事”。当变更注册成为最大块的批准类型,企业的质量体系、供应链一致性、上市后风险管理能力,会比单一产品的技术参数更能决定估值韧性。1
4)落地难点与争议:审批跑得快,临床与采购接得住吗
争议的核心不在“批不批”,而在“批完之后怎么用”。从数据看,2024年延续注册同比已连续下行(4722项,同比-1.4%),但变更注册与首次注册仍在上行。2这意味着产品迭代更频繁,监管与机构都要面对更高的版本管理成本。
更现实的难点在于证据标准的解释空间。欧洲MDR/IVDR的瓶颈已证明:临床/性能评价一旦成为公告机构的主要挑战点,证书会大面积延迟。4中国在加速创新获批的同时,也需要更清晰地把“可验证的临床获益”落实到真实使用场景里,否则审批侧的增量会在临床端变成“选择困难”,在支付端变成“控费冲突”。
5)结语:2026年的胜负手,可能不在“新证”,而在“新证之后”
2025年的数据把趋势写得很直白:审批总量上行只是表象,变更注册占比抬升与优先审批陡增,才是行业进入全生命周期竞争的标志。1下一阶段的关键问题是:企业能否把合规、证据与支付逻辑前置到研发;医院能否把评估与应用流程工业化。答案将决定“创新红利”最终落在谁手里。
参考文献
《2025年度医疗器械注册工作报告》,国家药监局,2026-02-24。https://www.nmpa.gov.cn/directory/web/nmpa/xxgk/fgwj/gzwj/gzwjylqx/20260224172356196.html
《2024年度医疗器械注册工作报告》,国家药监局,2025-02-13。https://www.nmpa.gov.cn/xxgk/fgwj/gzwj/gzwjylqx/20250213095700131.html
《2023年度医疗器械注册工作报告》,国家药监局,2024-02-05。https://www.nmpa.gov.cn/xxgk/fgwj/gzwj/gzwjylqx/20240205112550112.html?type=pc&m=
MedTech Europe,(PDF)。https://www.medtecheurope.org/wp-content/uploads/2025/01/mte_report_ivdr_mdr_2024-v7.pdf