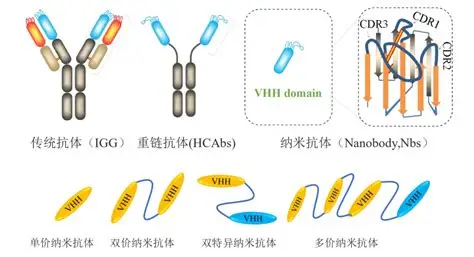
传统 IgG 抗体由两条重链与两条轻链组装而成,链间依靠二硫键稳定连接。重链与轻链均包含可变区和恒定区,其中重链恒定区分为 CH1、CH2、CH3,可变区为 VH;轻链包含恒定区 CL 与可变区 VL。抗体可变区存在氨基酸高度变异的高变区,共同组成抗原结合区域,决定 IgG 对抗原的识别特异性,是抗体发挥靶向结合功能的核心结构。
骆驼体内天然存在一种特殊的重链抗体 HCAb,这类抗体缺失轻链与重链 CH1 结构,仅保留 CH2、CH3 及重链可变区。其单一重链可变区即为最小抗原结合功能单元,被称作纳米抗体(VHH/Nb)。纳米抗体分子量约 15 ku,仅为传统 IgG 抗体的十分之一,在分子尺寸与结构组成上具备天然优势。VHH 主要依靠CDR1、CDR2、CDR3三个互补决定区结合抗原,也称为高变区,氨基酸序列高度多样;高变区之外骨架区 FR 序列保守稳定,且骆驼 VHH 骨架区与人源 VH 同源性可达 80% 以上,有效降低临床应用的免疫原性风险。
传统抗体 VH 结构中,特定疏水氨基酸位点会形成 VH 与 VL 的结合界面,单独表达 VH 时易因疏水区域暴露发生聚集沉淀。而骆驼 VHH 通过关键位点的氨基酸亲水改造,同时将 FR2 区域疏水性亮氨酸替换为亲水性丝氨酸,大幅降低蛋白聚集倾向,显著提升可溶性与理化稳定性,完美弥补了缺失轻链带来的结构缺陷。
一、互补决定区的结构差异除骨架区保守位点改造外,VHH 与普通 VH 在高变区的长度、残基组成和空间构象上存在明显区别。VHH 的 HV1 序列更长,新增氨基酸残基形成独特 β 转角,既优化分子溶解性,又拓展抗原结合界面;HV2 结构多样,部分呈现特殊折叠构象,进一步丰富结合模式。
二者最核心的差异集中在 HV3 区域。骆驼 VHH 的 CDR3 序列更长,能够形成凸起环状结构,深入抗原内部隐匿表位完成结合,弥补无轻链辅助结合的不足,实现传统抗体无法识别的特殊靶点结合。同时 VHH 高变区疏水氨基酸分布合理,表面静电分布均衡,进一步优化了分子溶解性与折叠稳定性。
二、纳米抗体 VHH 的整体结构与功能特性在三级结构层面,VHH 与普通 VH 整体折叠模式相近,均由反向平行 β 折叠片形成桶装空间结构,三个互补决定区集中分布在分子一端,保障抗原识别基础。但二者表面理化性质差异显著,VH 局部疏水残基集中,单独表达易聚集沉淀;而 VHH 表面亲水性残基分布均匀,溶解性更强、耐酸碱与耐高温性能更优。
纳米抗体作为极简的抗原结合单元,具备多项独特优势。分子尺寸微小,组织穿透性强,可高效渗透实体肿瘤组织;体内代谢快,能够通过肾脏快速清除,减少长期蓄积毒性;人源化程度高,免疫原性弱,适配体内靶向治疗。同时,VHH 高变区结构灵活多变,结合模式丰富,可结合抗原平面、裂隙及隐蔽空腔等多种表位。部分纳米抗体还会形成额外二硫键或特殊 α 螺旋结构,进一步稳定环区构象,提升结合亲和力与结构稳定性,使其在靶向药物、诊断试剂、基础研究等领域具备广阔应用价值。