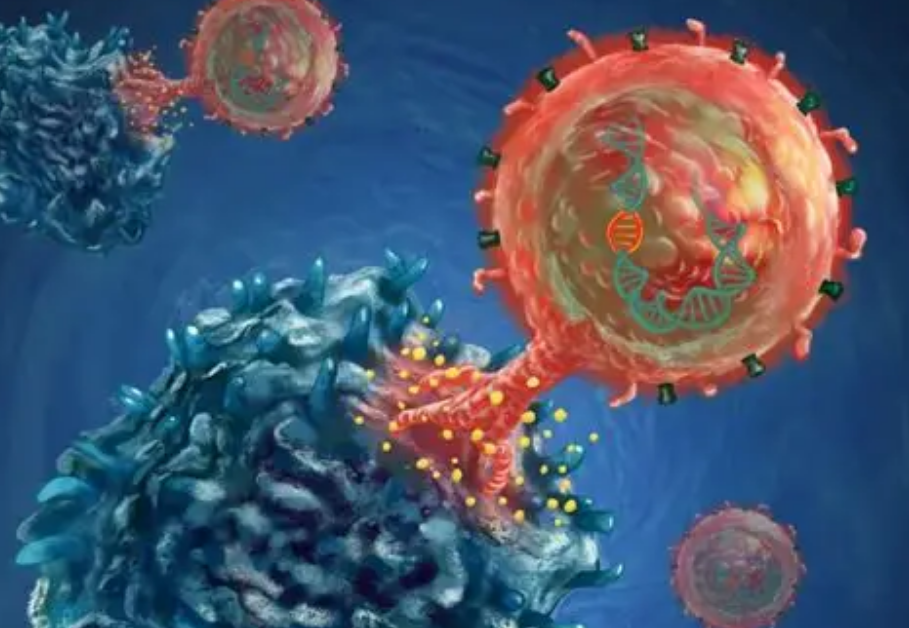
细胞免疫疗法,通俗来讲就是利用人体自身免疫细胞,通过基因修饰增强其抗肿瘤活性,进而精准杀伤癌细胞的新兴技术,CAR-T、CAR-NK、TCR-T 是其中的核心技术方向,而 CAR-T 疗法凭借其卓越的靶向性与杀伤效率,成为肿瘤免疫治疗领域的研究热点。
一、CAR-T 技术的核心:给 T 细胞装上 “精准导航”CAR-T,即嵌合抗原受体 T 细胞免疫疗法,其本质是通过基因工程技术,为人体免疫主力军 ——T 细胞,加装一个能精准识别癌细胞的 “嵌合抗原受体(CAR)”,让原本对癌细胞 “视而不见” 的 T 细胞,变身成特异性杀伤肿瘤的 “精准杀手”。
1. CAR 的三大核心组成部分一个完整的 CAR 结构,就像一套精密的作战系统,由三部分协同作用:
外部抗原识别结构:即阳性信号复合物(PCS),核心是单链抗体。这部分是 CAR-T 细胞的 “雷达”,能够特异性识别并结合肿瘤细胞表面的抗原(如 CD19),实现对癌细胞的精准定位。
内部信号传导模块:由 CD3ζ 链和 1-2 个共刺激分子(如 CD28、4-1BB)组成。当 “雷达” 锁定目标后,这部分会迅速传递激活信号,触发 T 细胞的增殖与活化,相当于作战系统的 “指挥中枢”。
负向调节模块:如 CD28 内柄结构。其作用是 “刹车”,避免 T 细胞被过度激活,平衡杀伤活性与安全性,降低免疫风暴等副作用的风险。
2. CAR-T 细胞的杀伤原理T 细胞是来源于骨髓造血干细胞、在胸腺中发育成熟的免疫细胞,负责监控和清除体内异常细胞。经过 CAR 修饰的 T 细胞,会通过以下步骤发挥作用:
CAR 的 “雷达” 识别并结合肿瘤细胞表面抗原;
信号传导模块启动,激活 T 细胞的杀伤程序;
活化的 CAR-T 细胞释放大量细胞毒素,直接裂解癌细胞;
同时,CAR-T 细胞会快速增殖,形成长效免疫记忆,防止肿瘤复发。
二、CAR-T 技术的四代进化:从低效到精准的迭代之路CAR-T 技术的发展,是一个不断优化结构、提升疗效与安全性的过程,至今已历经四代迭代:
第一代 CAR-T:核心结构仅包含 CD3ζ 链的 ITAM 信号区,能传递基础激活信号,但缺乏共刺激信号,导致 T 细胞增殖能力弱、体内存活时间短,临床疗效未达预期。
第二代 CAR-T:在第一代基础上,加入了 CD28 或 4-1BB 等共刺激分子。这一改进极大增强了 T 细胞的活化、增殖与存活能力,在临床中展现出突破性疗效,成为目前应用最广泛的 CAR-T 版本。不过,其载体(逆转录病毒)的基因容量有限,无法同时搭载两种共刺激分子。
第三代 CAR-T:采用慢病毒作为载体,可搭载两个及以上共刺激分子,理论上能进一步强化信号传导。但临床研究显示,其杀伤活性并未显著提升,且可能增加过度激活的风险。
第四代 CAR-T(精准 CAR-T):聚焦于解决临床应用中的安全性与有效性瓶颈,是新一代研发方向。一方面,通过引入自杀基因,实现对 CAR-T 细胞的可控 “开关”,降低脱靶效应与免疫风暴风险;另一方面,添加细胞因子或趋化因子受体结构,增强 CAR-T 细胞向肿瘤组织的浸润能力,提升实体瘤治疗效果。
三、CAR-T 疗法的临床应用流程与适应症1. 标准化治疗流程CAR-T 疗法是一套 “个性化定制” 的治疗方案,核心流程分为五步:
适应症评估:判断患者是否符合 CAR-T 治疗条件(如肿瘤抗原表达阳性);
细胞采集:从患者外周血中分离出 T 细胞;
基因修饰:通过病毒载体将 CAR 基因导入 T 细胞,使其表达嵌合抗原受体;
体外扩增:在实验室中大量培养扩增 CAR-T 细胞,达到治疗所需剂量;
回输与监测:将扩增后的 CAR-T 细胞回输患者体内,全程监控患者的免疫反应与治疗效果。
回输后的 CAR-T 细胞可在体内存活数月至数年,形成长期免疫保护。
2. 主要临床应用领域目前,大部分 CAR-T 疗法仍处于临床试验阶段,但在部分血液肿瘤治疗中已获批上市,核心适应症集中在:
复发或难治性急性 B 系淋巴细胞白血病;
两种及以上治疗方案失败的大 B 细胞非霍奇金淋巴瘤;
CD19 阳性复发、难治性恶性淋巴瘤;
CD19 治疗失败后,CD22 阳性的急性淋巴细胞白血病。
在实体瘤领域,CAR-T 疗法的相关研究正在推进,但受限于肿瘤微环境、靶点特异性等问题,疗效尚未明确。
四、CAR-T 技术的前景与挑战作为肿瘤免疫治疗的革命性技术,CAR-T 疗法为复发难治性血液肿瘤患者带来了治愈希望,其应用前景广阔 —— 未来可通过靶点优化、联合治疗(如与免疫检查点抑制剂联用)、通用型 CAR-T 开发等方向,拓展实体瘤治疗边界,降低治疗成本。
但 CAR-T 技术的发展仍面临诸多挑战:实体瘤浸润困难、脱靶效应与免疫风暴等副作用、治疗成本高昂、通用型细胞制备技术尚未成熟等问题,仍是制约其广泛应用的关键瓶颈。随着技术的不断突破与优化,CAR-T 疗法有望在肿瘤精准治疗领域发挥更大价值。